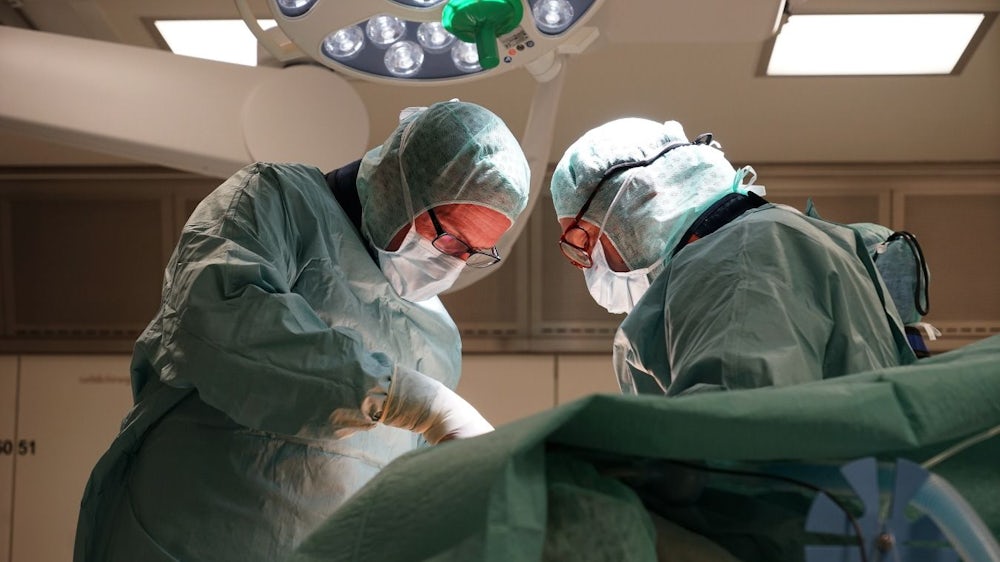
Die kleinen, filigranen Teile können Kinderleben retten - doch sie sind knapp: Kliniken haben Probleme, manche spezialisierte Medizinprodukte nachzubestellen, etwa Ballonkatheter und Stents für Kinder. Auch bei anderem wichtigen Handwerkszeug drohe Mangel, warnen Ärztevertreter, zum Beispiel bei bestimmten Skalpellen, Endoskopen oder Herzklappen. Schuld daran ist nach Ansicht dieser Kritiker vor allem ein EU-Gesetz, die neue Medizinprodukte-Verordnung. Am Freitag reagierte die Kommission auf das monatelange Drängen von Verbänden und Europaabgeordneten und schlug vor, Übergangsfristen für den Rechtsakt zu verlängern.
EU-Parlament und Ministerrat, die Gesetzgebungskammer der Mitgliedstaaten, müssen den Änderungen noch zustimmen; dies soll in einem beschleunigten Verfahren geschehen. Gesundheitskommissarin Stella Kyriakides sagte, "mehrere Umstände" hätten "dazu geführt, dass den Gesundheitssystemen in der gesamten EU Engpässe bei lebensrettenden Medizinprodukten" drohten. Die vorgeschlagenen Anpassungen sollten sicherstellen, dass "kurzfristig jegliches Risiko von Engpässen verringert und der Zugang für die am meisten auf diese Produkte angewiesenen Patientinnen und Patienten gewährleistet wird".
Hinter den Querelen steht die Verschärfung der Medizinprodukte-Verordnung. Die wurde schon 2017 beschlossen, als Lehre aus dem Skandal um minderwertige Brustimplantate in Deutschland und Frankreich. Doch erst seit 2021 gelten die härteren Regeln. Das Gesetz verlangt, dass Hersteller ihre Medizinprodukte bis Mai 2024 neu zulassen, ansonsten erhalten sie nicht das notwendige CE-Zeichen, das belegt, dass die Waren EU-Standards entsprechen. Aber diese Neuzulassung ist aufwendig, teuer und langwierig - sie dauert zwischen 13 und 18 Monaten. Daher ist es nicht zu schaffen, bis 2024 sämtliche Produkte neu zu zertifizieren.
Manche Anbieter entscheiden auch, dass sich die Mühe für Nischenprodukte gar nicht lohnt. Die Waren verschwinden dann früher oder später vom Markt. Eine Erhebung des Deutschen Industrie- und Handelskammertags und anderer Verbände unter 378 Firmen ergab, dass in 16 der 21 abgefragten Produktgruppen mindestens die Hälfte der Unternehmen einzelne Produkte oder gar komplette Sortimente streiche: zum Beispiel in der Orthopädie oder bei chirurgischen Instrumenten.
Firmen hätten sich "nicht ausreichend vorbereitet", heißt es
Ein weiteres Problem ist, dass es zu wenige Benannte Stellen gibt. So heißen die Prüfeinrichtungen, an die sich die Konzerne für die Zulassung wenden müssen, etwa der Tüv Süd. Die EU-Verordnung verlangt auch von den Benannten Stellen, sich neu zertifizieren zu lassen, bevor sie gemäß den verschärften Regeln prüfen dürfen. Das zieht sich jedoch hin, bislang haben das EU-weit nur 36 Einrichtungen geschafft - und die kommen nun mit der Arbeit nicht nach.
Die Kommission schlägt daher jetzt vor, den Herstellern mehr Zeit für die Zertifizierung zu geben. Die Frist soll von Mai 2024 auf Dezember 2027 verlängert werden, für Güter mit geringem Risiko wie Spritzen sogar bis Ende 2028. Außerdem soll die bestehende Zulassung von Produkten nicht automatisch auslaufen; Krankenhäuser müssen also keine knappen Katheter wegwerfen, bloß weil die Zertifizierung schon so lange her ist. Viele Hersteller hätten sich "nicht ausreichend vorbereitet", klagt die Brüsseler Behörde. Der Bundesverband Medizintechnologie (BVMed) widerspricht und erklärt, die Branche bereite "sich seit Jahren intensiv" vor; die Umsetzung koste geschätzt zwischen sieben und zehn Milliarden Euro. BVMed-Geschäftsführer Marc-Pierre Möll begrüßt den Aufschub und fordert, "diese gesetzgeberischen Maßnahmen zügig umzusetzen".
Die CSU-Europaabgeordnete Angelika Niebler, Co-Vorsitzende von CDU/CSU im Straßburger Parlament, nennt den Vorstoß der Kommission "einen wichtigen Schritt hin zu mehr Patientensicherheit" in der EU: "Unser monatelanger Druck auf die Kommission, das Problem anzugehen, ist endlich erfolgreich."