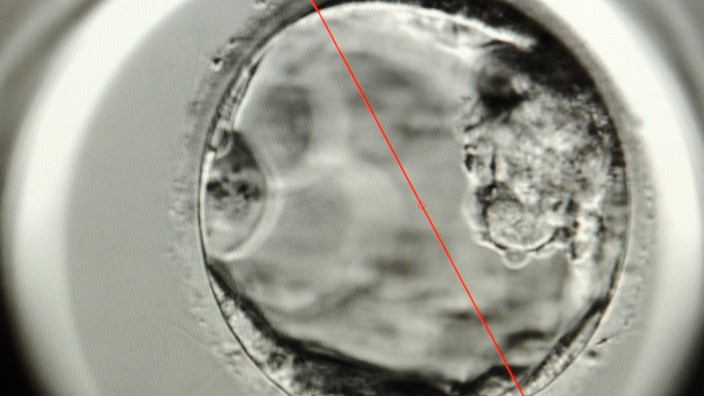
Zwei Jahre sind in der Wissenschaft eine ziemlich kurze Zeit. Insbesondere dann, wenn innerhalb dieser 24 Monate nicht einfach nur Experimente fortgesetzt und dabei ein bisschen weiterentwickelt werden. Sondern wenn Forscher etwas völlig Neues probieren. Und es tatsächlich auch noch funktioniert.
Der britischen Entwicklungsbiologin Kathy Niakan ist dieses Kunststück gelungen. Vor wenigen Tagen hat die Nachwuchsforscherin vom Francis Crick Institute in London die weltweit erste Arbeit publiziert, für die gezielt in die Genetik der menschlichen Embryonalentwicklung eingegriffen wurde. Wie Niakans Team in der aktuellen Ausgabe des Fachjournals Nature berichtet, können Defekte in einem Gen namens Oct-4 das Wachstum von sehr frühen Embryonen massiv stören und eine normale Entwicklung unterbinden.
Die Erkenntnis könnte künftig dabei helfen, die Erfolgsrate von künstlichen Befruchtungen zu erhöhen - und zu verstehen, warum auch die natürliche Fortpflanzung so selten erfolgreich verläuft. Tatsächlich kommt es bei sieben von acht im Körper befruchteten Eizellen nicht zu einer stabilen Schwangerschaft.
Der heimliche Superstar der Studie aber heißt wieder einmal Crispr-Cas. Die Genschere beschleunigt die Arbeit in den Lebenswissenschaften derart, dass kaum noch Zeit zum Innehalten bleibt. Insbesondere nicht für die Ethiker, für die der Eingriff in die menschliche Keimbahn ein besonders heikles Feld ist. Zwei Jahre ist es erst her, dass Niakan die erste Erlaubnis zur genetischen Veränderung von lebensfähigen menschlichen Embryonen erhalten hat.
Großbritannien hatte sich mit der Erlaubnis im September 2015 als erstes Land offiziell dazu bekannt, zumindest experimentell in das Erbgut des Menschen eingreifen zu wollen. Versuche an überzähligen Embryonen aus künstlichen Befruchtungen waren zwar schon zuvor in engen Grenzen gestattet gewesen, aber eben nicht der Griff in die Gene. Die Entscheidung hatte 2015 für großes Aufsehen gesorgt und massive Kritik geerntet.
Die Ergebnisse mit Mäusen lassen sich nicht auf Menschen übertragen
Für deutsche Wissenschaftler haben die britischen Genexperimente an menschlichen Embryonen aber noch eine besonders schmerzhafte Erkenntnis zu bieten: Obwohl sich andere Säugetiere für grundsätzliche Forschungen zur Embryonalentwicklung sehr wohl eignen, zeigen die Experimente von Niakan auch sehr deutlich, dass diese Vergleichbarkeit Grenzen hat. So wurde das jetzt als so wichtig erkannte Gen Oct-4 1990 zwar vom deutschen Stammzellforscher Hans Schöler in der Maus entdeckt.
Wie die aktuelle Arbeit jetzt belegt, spielt es in der Embryonalentwicklung des Menschen allerdings eine etwas andere Rolle als in dem häufig genutzten Versuchstier. "Obwohl sich die Embryonen von Maus und Mensch sehr ähnlich sind, zeigt diese Arbeit, dass man beides untersuchen muss", sagt die Embryologin Magdalena Zernicka-Götz von der britischen University of Cambridge. In Deutschland ist die Forschung an Embryonen jedoch verboten.
Man konnte die Wehmut der hiesigen Forschergemeinde am Wochenende nach der Veröffentlichung fast greifen. Niakans Vorgesetzter, Robin Lovell Badge, war aus London nach Halle an der Saale gereist, um über Für und Wider des Genome Editing in der Keimbahn zu sprechen. Aus gegebenem Anlass jedoch berichtete er über die Studie seiner Mitarbeiterin, zeigte Kurzfilmchen von wachsenden Zellkugeln, die sich normal oder eben nicht normal entwickelten, und erklärte weitere Details des eleganten Experiments.
Die Wehmut, sie kann eigentlich nur weiter wachsen
Es blieb bei der rein wissenschaftlichen Betrachtung, die ohnehin nur wenige Gründe gegen den Eingriff in die Keimbahn kennt. Entscheidend ist die Ethik. Und in Deutschland das Embryonenschutzgesetz. Keine dieser Forschungen wäre in der Bundesrepublik möglich. Jeder deutsche Forscher, der sich wissentlich an solchen Experimenten im Ausland beteiligt, macht sich strafbar.
Die Wehmut, sie kann eigentlich nur weiter wachsen. Während die deutschen Restriktionen und die gesellschaftliche Ablehnung gegenüber der Forschung an Embryonen und der Gentechnik wenig Hoffnung darauf lassen, dass die hiesige Wissenschaft im Wettlauf um neue Erkenntnisse vielleicht doch noch eine Rolle spielen wird, denkt man anderswo schon sehr viel weiter. In den Vereinigten Staaten etwa hat die Defense Advance Research Projects Agency, kurz Darpa, vor einigen Wochen angekündigt, in den kommenden Jahren 65 Millionen Dollar in ein Projekt zum Genome Editing zu investieren.
"Ein Teil der Herausforderung und des Engagements besteht für uns darin, uns einen Reim auf die ethischen Implikationen der Gene Editing Technologien zu machen, die Bedenken der Bevölkerung zu verstehen und unsere Forschung proaktiv daran zu orientieren, so dass die Interessenvertreter mit Daten zur Entscheidungsfindung ausgestattet sind", sagte Projektleiterin Renee Wegzryn zum Start von Safe Genes.
Ihre Themen kreisen weder um Embryonen, noch um neue Pflanzenzüchtungen
Doch inwiefern die Frage nach der Ethik hier wirklich vorrangig behandelt wird, bleibt abzuwarten. Die Darpa hat als Agentur des US-Verteidigungsministeriums sieben Teilprojekte angekündigt, geleitet unter anderem von einer der Crispr-Erfinderinnen, Jennifer Doudna von der University of California in Berkeley, von George Church von der Harvard Medical School in Boston und von Kevin Esvelt vom Massachusetts Institut of Technology im amerikanischen Cambridge.
Ihre Themen kreisen weder um Embryonen, noch um neue Pflanzenzüchtungen, sondern um die Frage, wie sich Gene-Editing-Technologien kontrollieren lassen. Ein Beispiel sind sogenannte Daisy Drives, eine Weiterentwicklung der sogenannten Gene Drives. Es handelt sich bei den Gene Drives um sich selbst vermehrende Genscheren, die zum Beispiel ins Genom von Mücken eingebaut werden sollen, um die Verbreitung von Krankheiten wie Malaria zu stoppen. Auch diese Technik ist umweltethisch derart umstritten, dass der Deutsche Ethikrat dem Thema im Oktober eine komplette Veranstaltung widmen wird.
Vielleicht ist das alles aber auch schon zu spät, denn die Amerikaner haben nun mal längst andere Anwendungen im Visier: Im Gegensatz zum Original, welches einmal in die Welt gesetzt unaufhaltsam seine Arbeit ausführt, bis der Zielorganismus resistent geworden oder ausgestorben ist, sollen die Daisy Drives es ermöglichen, die Gene Drives exakt zu steuern, geografisch zu begrenzen und auch wieder rückgängig zu machen. Was sinnvoll klingt. Man muss aber hoffen, dass es sich bei den veränderten Organismen dann auch künftig nur um Mücken handelt. Denkbar wäre noch viel mehr.