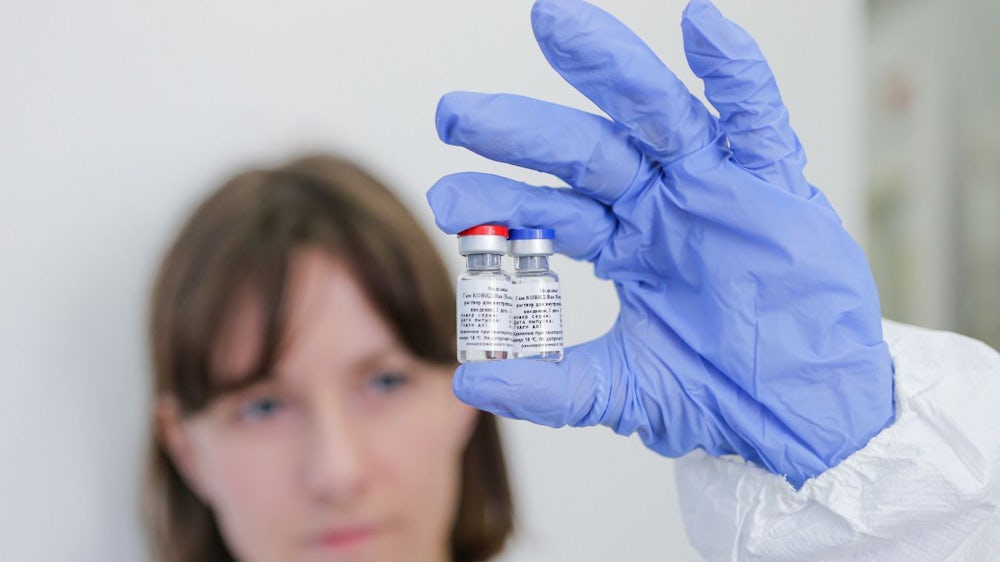
Lange angekündigt und dennoch überraschend war, was der russische Präsident am Dienstag bekannt gab: Vor allen anderen Kandidaten lässt Russland einen Impfstoff gegen das neue Coronavirus zu. Obwohl eine Wirksamkeitsstudie fehlt und die bislang vorhandenen Verträglichkeitsdaten von weit weniger als 100 Versuchspersonen nicht publiziert sind, hat "Sputnik V" laut Wladimir Putin alle "erforderlichen Prüfungen bestanden". "Sputnik V" soll der Vermarktungsname des Impfstoffs sein - in Reminiszenz an 1957, als die damalige Sowietunion mit einem Satelliten die erste Etappe des Raumfahrt-Wettlaufs zwischen Russen und Amerikanern gewann.
Seit der Ankündigung sind nun neue Informationen über den Impfstoff und seine Zulassung bekannt geworden. Das Wissenschaftsjournal Science berichtet, dass das Zulassungszertifikat des Impfstoffs Einschränkungen enthält. Demnach sollen vorläufig nur besonders "anfällige" Personen den Impfstoff erhalten. Eine Impfkampagne in der Bevölkerung dagegen darf demnach erst mit dem Jahreswechsel beginnen. Letzteres allerdings wäre angesichts einer Einwohnerzahl von rund 145 Millionen wohl auch gar nicht früher möglich, denn der russische Hersteller der Impfstoffs, Binnopharm, hat angekündigt, zunächst nur 1,5 Millionen Impfdosen pro Jahr herstellen zu können.
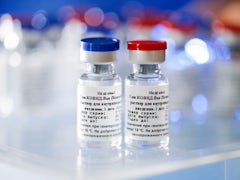
Wladimir Putins Tochter soll bereits damit immunisiert worden sein. Ob die Impfung wirkt und sicher ist, bleibt allerdings weiter unklar.
Das Mittel enthält Viren, die Infektionen verschlimmern könnten
Diskussionen gibt es unterdessen weiterhin um die fehlenden klinischen Tests der sogenannten Phase 3. Sowohl für Medikamente als auch Impfstoffe werden in den ersten zwei klinischen Prüfungsabschnitten lediglich die Verträglichkeit, häufige Nebenwirkungen und Hinweise auf eine mögliche Wirkung an einer geringen Zahl von Probanden untersucht. Erst in der dritten Phase werden Wirksamkeit und Nebenwirkungen eines Mittels an einer großen Zahl von Freiwilligen geprüft. Die Teilnehmer stellen dabei zumeist einen Querschnitt der späteren Zielgruppe dar. Seltene Nebenwirkungen, die schwer oder lebensbedrohlich sein können, zeigen sich allerdings erst ab einer Teilnehmerzahl von etlichen Tausend Probanden. Russland plant im Nachgang der Zulassung eine Phase-3-Studie an lediglich 2000 Menschen.
Gerade im Fall von Gam-Covid-Vac Lyo, wie das Vakzin des Moskauer Gamaleya-Instituts eigentlich heißt, gibt es jedoch Hinweise darauf, dass besonders gravierende Nebenwirkungen auftreten könnten. So wird der Impfstoff in zwei Dosen verabreicht, die sogenannte Adenoviren enthalten. Diese Viren dienen als Verpackung - man sagt auch Vektor - für Informationen über den eigentlichen Gegner, das Coronavirus. Adenoviren selbst sind dabei eigentlich harmlos, allerdings können sie als Vektor in Impfstoffen auch zur Folge haben, dass die Probanden nicht immun, sondern noch anfälliger für eine Infektion werden. 2007 wurden deshalb Tests an einem vektorbasierten Impfstoff gegen den Aidserreger HIV abgebrochen.
Auch wegen dieser Hintergründe ist die Kritik an der Zulassung selbst im eigenen Land harsch. Die Vorsitzende der russischen Vereinigung klinischer Forschungsorganisationen sagte in Science, sie schäme sich für ihr Land. Die Vereinigung hatte bis zum Schluss versucht, die Zulassung zu verhindern.