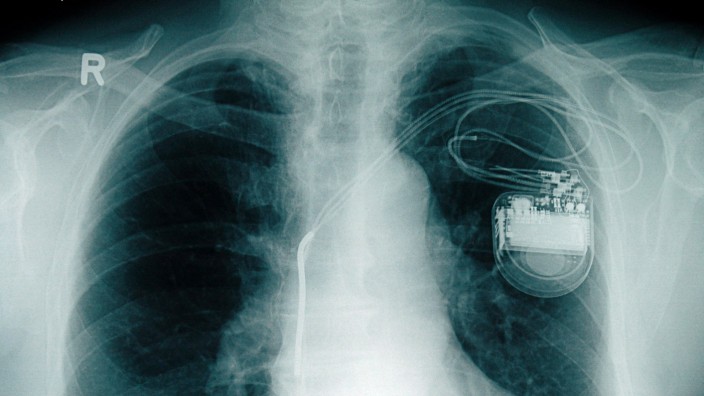
Wie entscheidend eine Bewertung auch von medizinischen Produkten ist, belegt vielleicht am besten das kürzlich bekannt gewordene Beispiel Nanostim. Dabei handelt es sich um einen Herzschrittmacher, der, anders als die Konkurrenzprodukte, direkt in die rechte Herzkammer implantiert wird. Er benötigt deshalb keine Elektroden. Und auch zu der sichtbaren Ausbeulung an der Brust, wo die herkömmlichen Schrittmacher eingesetzt werden, kommt es nicht.
Ende 2013 wurde Nanostim in den Markt eingeführt und begeistert aufgenommen. Nach Recherchen des Bayerischen Rundfunks wurden in Deutschland etwa 200 Patienten mit der neuen Methode behandelt. Immer wieder gab es Komplikationen. Anfang 2015 rief der Hersteller das Produkt zurück und stoppte den Vertrieb. "Bei der europäischen Postmarketingstudie kam es in rund 3,4 Prozent der Fälle, bei denen diese neue Form des Herzschrittmachers eingesetzt wurde, zu Blutungen in den Herzbeutel", urteilt die Vorsitzende des Spitzenverbandes der Gesetzlichen Krankenkassen, Doris Pfeiffer.
In einigen Fällen sei der Herzmuskel beim Befestigen des Schrittmachers von innen durchstoßen worden, sagte Pfeiffer der Süddeutschen Zeitung. "Manche Patienten starben in direktem Zusammenhang mit diesem neuen Schrittmacher, und wir gehen davon aus, dass das bei einem klassischen Schrittmacher nicht der Fall gewesen wäre."
Solche Fälle sollen nun nicht mehr vorkommen. Die große Koalition will in ihrem Versorgungsstärkungsgesetz eine automatische Nutzen-Bewertung auch für Medizinprodukte einer hohen Risikoklasse einführen. Das heißt, es geht um solche Dinge wie eben Herzschrittmacher, aber auch um Gelenk-Implantate, um Stents und um Silikoneinlagen bei Brust-OPs. Zusätzliche Bedingung für die Prüfung ist, dass sich die ganze Prozedur von den üblichen unterscheidet. Sie muss mit einem "neuen theoretisch-wissenschaftlichen Konzept" verbunden sein, heißt es. Nach zwei Jahren sollen dann ausreichende Studien vorliegen, um das neue Produkt und seine Anwendung zu beurteilen.
"Die neue Regelung ist ein großer Schritt in die richtige Richtung", lobt GKV-Chefin Pfeiffer. Die Koalition wolle einen Automatismus zur Nutzen-Prüfung einrichten, der festen Fristen folge und schnell durchlaufen werden könne. "Das finden wir gut." Dennoch befürchtet Pfeiffer, dass die geplante Neuregelung zwei zentrale Webfehler aufweist, die ihre Wirkung beeinträchtigen könnten.
Nach den bisherigen Plänen der Koalition sollen die Kassen die Anwendung auch dann schon bezahlen, wenn sie noch nicht erprobt wurde, und sie sollen darüber hinaus auch die Anwendungskosten für Patienten finanzieren, die nicht an der Studie teilnehmen. Nach Pfeiffers Worten wäre diese Regelung kontraproduktiv. "Die Krankenhäuser hätten keinen Anreiz, die Studie schnell fertigzustellen." Müssten die Kassen lediglich die Kosten für die Studienteilnehmer erstatten, würde das die Sache beschleunigen. Sprich, die Kliniken hätten einen Anreiz, die Studie schnell abzuschließen, um später alle Patienten auf Kosten der Kassen zu behandeln.
Zudem seien die Bedingungen für die Teilnahme der Kliniken an den Studien nicht ausreichend scharf formuliert, sagte Pfeiffer. So gebe es auch die Möglichkeit, die Patienten im Rahmen einer Beobachtungsstudie zu behandeln, deren Auflagen laxer sind. "Es steht zu befürchten, dass die Krankenhäuser nur wenige Patienten in die richtige Studie einschließen und die anderen unter weniger kontrollierten Bedingungen behandeln", sagte Pfeiffer. Damit fehlten aber am Ende deren Daten bei der Auswertung, und somit bestehe die Gefahr, dass die Studie keine auswertbaren Ergebnisse bringt.